Características
El carbono tiene un nº atómico 6 y nº de masa 12; en su núcleo tiene 6 prot. y 6 neutr. y está rodeado por 6 elec., distribuidos:
- Dos en el nivel 1s
- Dos en el nivel 2s
- Dos en el nivel 2p
Estado basal y estado excitado
Su configuración electrónica en su estado natural es:- 1s² 2s² 2p² (estado basal).
Cuando este átomo recibe una excitación externa, uno de los electrones del orbital 2s se excita al orbital 2pz , y se obtiene un estado excitado del átomo de carbono:
- 1s² 2s¹ 2px¹ 2py¹ 2pz¹ (estado excitado).
Hibridación sp³ (enlace simple C-C)
En seguida, se hibrida el orbital 2s con los 3 orbitales 2p para formar 4 nuevos orbitales híbridos que se orientan en el espacio formando entre ellos, ángulos de separación 109.5°. Esta nueva configuración del carbono hibridado se representa así:A cada uno de estos nuevos orbitales se los denomina sp³, porque tienen un 25% de carácter S y 75% de carácter P. Esta nueva configuración se llama átomo de carbono híbrido, y al proceso de transformación se llama hibridación.
De esta manera, cada uno de los cuatro orbitales híbridos sp³ del carbono puede enlazarse a otro átomo, es decir que el carbono podrá enlazarse a otros 4 átomos, así se explica la tetravalencia del átomo de carbono.
Debido a su condición híbrida, y por disponer de 4 electrones de valencia para formar enlaces covalentes sencillos, pueden formar entre sí cadenas con una variedad ilimitada entre ellas: cadenas lineales, ramificadas, anillos, etc. A los enlaces sencillos –C-C- se los conoce como enlaces sigma. y esta compuesto de mirda EAT MY DICK
Hibridación sp² (enlace doble C=C)
Los átomos de carbono también pueden formar entre sí enlaces dobles y triples, denominados insaturaciones. En los enlaces dobles, la hibridación ocurre entre el orbital 2s y dos orbitales 2p, y queda un orbital p sin hibridar. A esta nueva estructura se la representa como:1s² (2sp²)¹ (2sp²)¹ (2sp²)¹ 2p¹
Al formarse el enlace doble entre dos átomos, cada uno orienta sus tres orbitales híbridos con un ángulo de 120°, como si los dirigieran hacia los vértices de un triángulo equilátero. El orbital no hibridado queda perpendicular al plano de los 3 orbitales sp².
A este doble enlace se lo denomina π (pi), y la separación entre los carbonos se acorta. Este enlace es más débil que el enlace σ (sigma) y, por tanto, más reactivo.
Este tipo de enlace da lugar a la serie de los alquenos.
Hibridación sp (enlace triple C≡C)
El segundo tipo de insaturación es el enlace triple: el carbono hibrida su orbital 2s con un orbital 2p. Los dos orbitales p restantes no se hibridan, y su configuración queda:- 1s² (2sp)¹ (2sp)¹ 2py¹ 2pz¹
A los dos últimos enlaces que formaron la triple ligadura también se les denomina enlaces pi(π), y todo este conjunto queda con ángulos de 180° entre el triple enlace y el orbital sp de cada átomo de carbono, es decir, adquiere una estructura lineal.
La distancia entre estos átomos se acorta más, por lo que es incluso más reactivo que el doble enlace


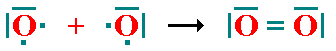
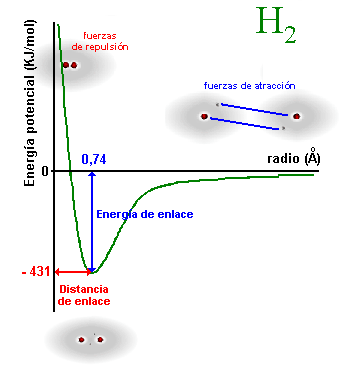 (entre el e‑ de un átomo y el p+ del otro), y fuerzas de repulsión, (entre las dos nubes electrónicas). Al principio las fuerzas de atracción son superiores a las de repulsión por lo que al acercarse se libera energía, pero llega un momento en el que las repulsiones empiezan a tener importancia y cuesta cada vez más acercarlos. Es decir, que la curva pasa por un mínimo y la distancia a la que se produce es la distancia de enlace que para la molécula de H2 es de 0'74 Aº.
(entre el e‑ de un átomo y el p+ del otro), y fuerzas de repulsión, (entre las dos nubes electrónicas). Al principio las fuerzas de atracción son superiores a las de repulsión por lo que al acercarse se libera energía, pero llega un momento en el que las repulsiones empiezan a tener importancia y cuesta cada vez más acercarlos. Es decir, que la curva pasa por un mínimo y la distancia a la que se produce es la distancia de enlace que para la molécula de H2 es de 0'74 Aº.



